Ar
ИЗОТОПЫ АРГОНА
B
ИЗОТОПЫ БОРА
W
ИЗОТОПЫ ВОЛЬФРАМА
Ge
ИЗОТОПЫ ГЕРМАНИЯ
Fe
ИЗОТОПЫ ЖЕЛЕЗА
Ir
ИЗОТОПЫ ИРИДИЯ
Cd
ИЗОТОПЫ КАДМИЯ
Si
ИЗОТОПЫ КРЕМНИЯ
Kr
ИЗОТОПЫ КРИПТОНА
Xe
ИЗОТОПЫ КСЕНОНА
Mo
ИЗОТОПЫ МОЛИБДЕНА
Ni
ИЗОТОПЫ НИКЕЛЯ
Sn
ИЗОТОПЫ ОЛОВА
Os
ИЗОТОПЫ ОСМИЯ
Pb
ИЗОТОПЫ СВИНЦА
Se
ИЗОТОПЫ СЕЛЕНА
S
ИЗОТОПЫ СЕРЫ
Te
ИЗОТОПЫ ТЕЛЛУРА
C
ИЗОТОПЫ УГЛЕРОДА
Cr
ИЗОТОПЫ ХРОМА
Zn
ИЗОТОПЫ ЦИНКА
Zr
ИЗОТОПЫ ЦИРКОНИЯ
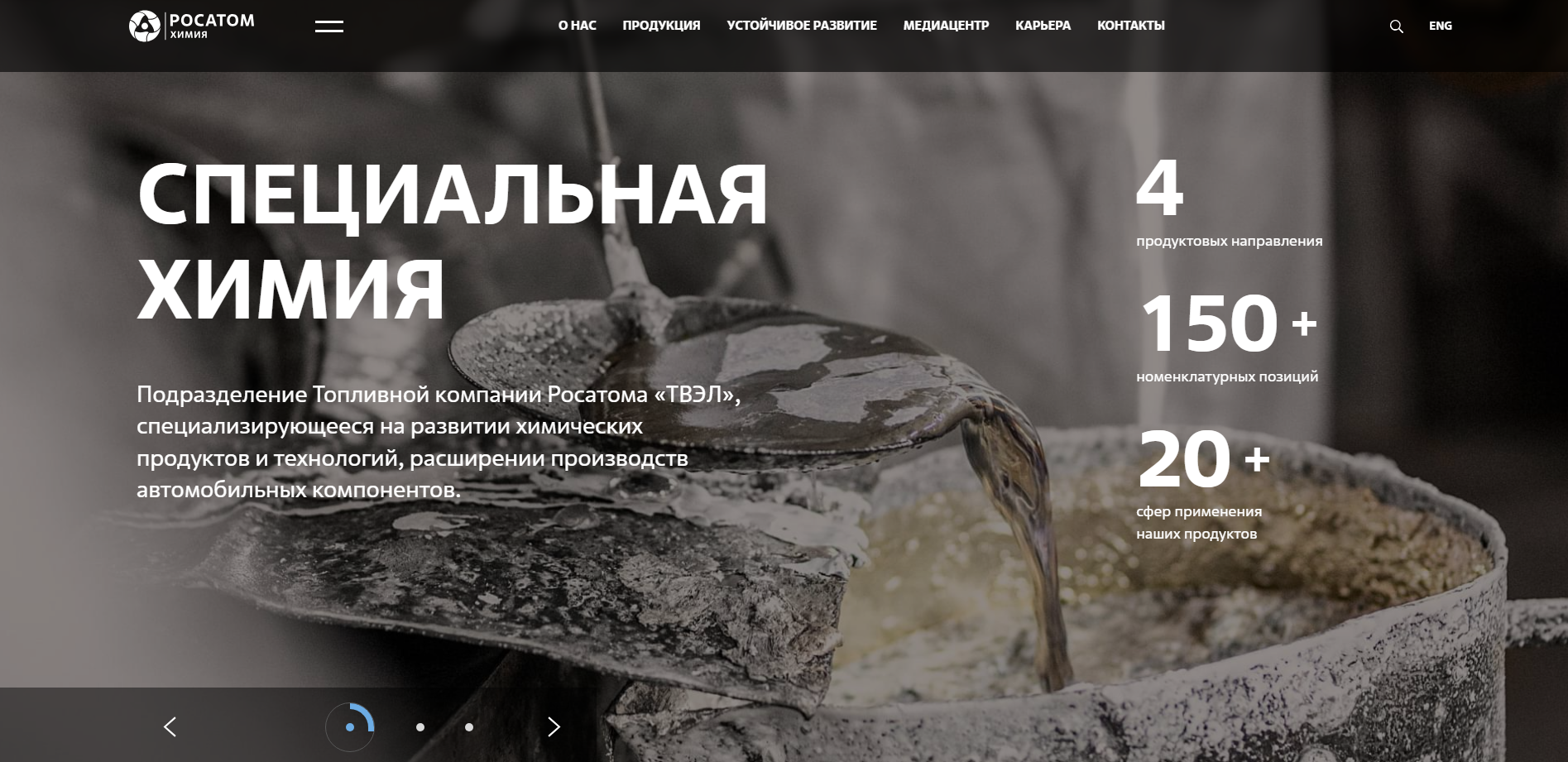
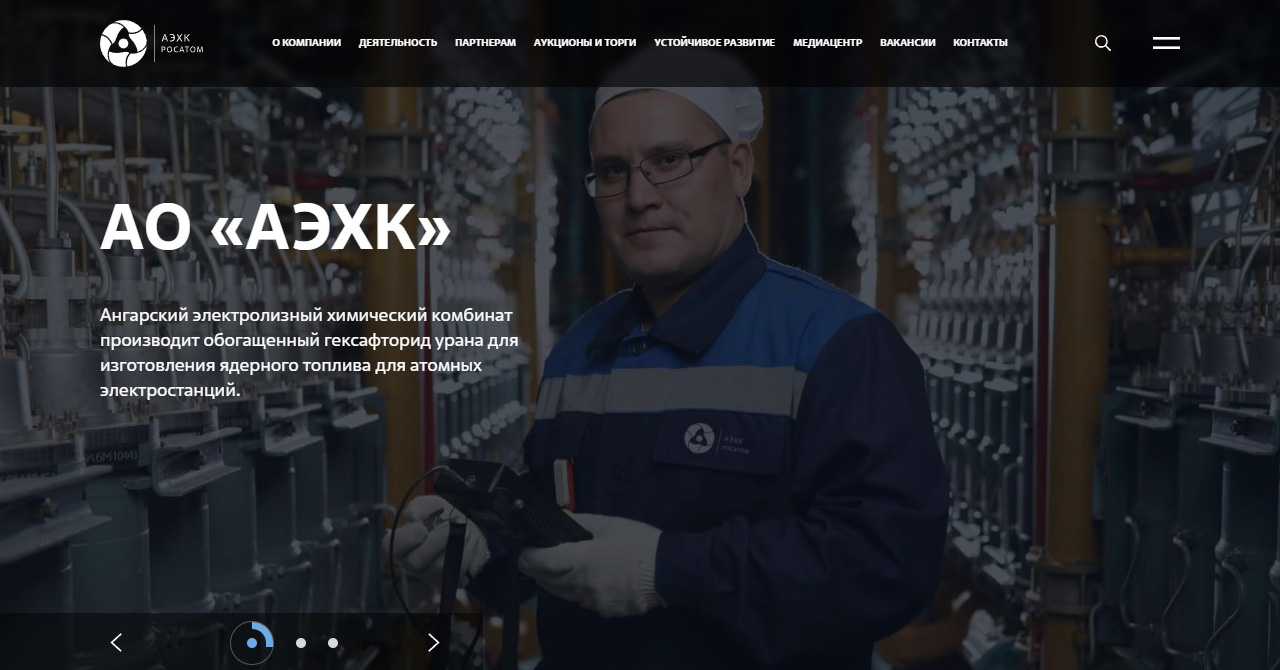
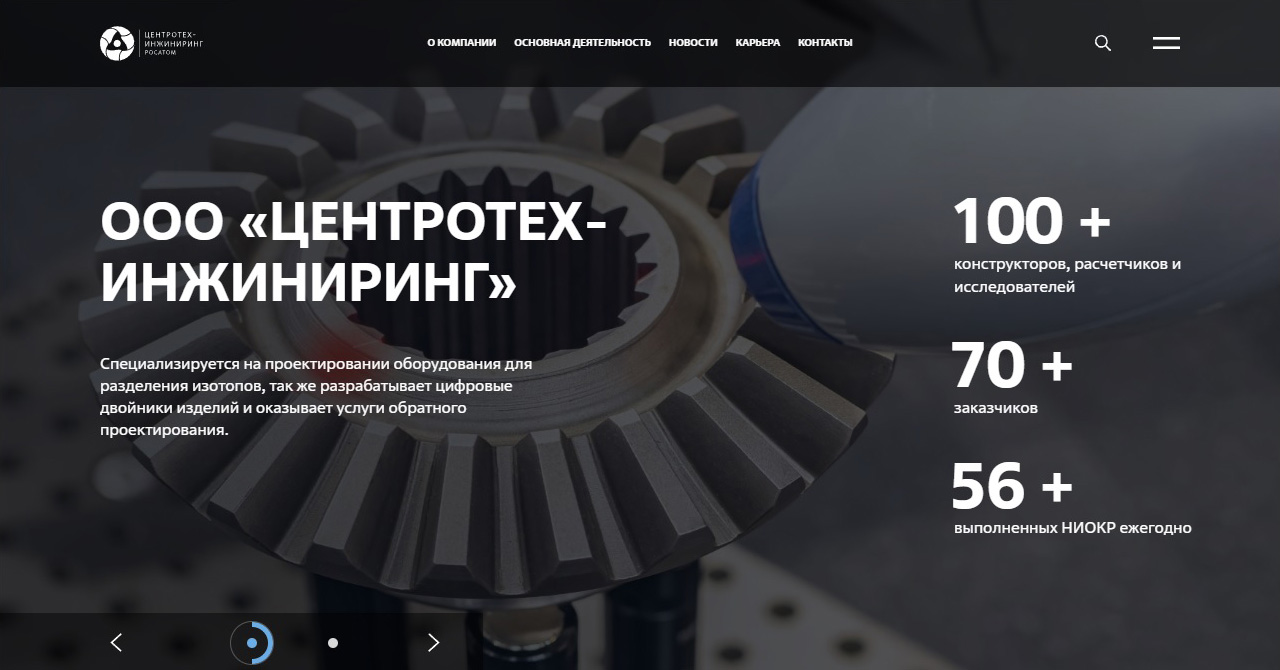
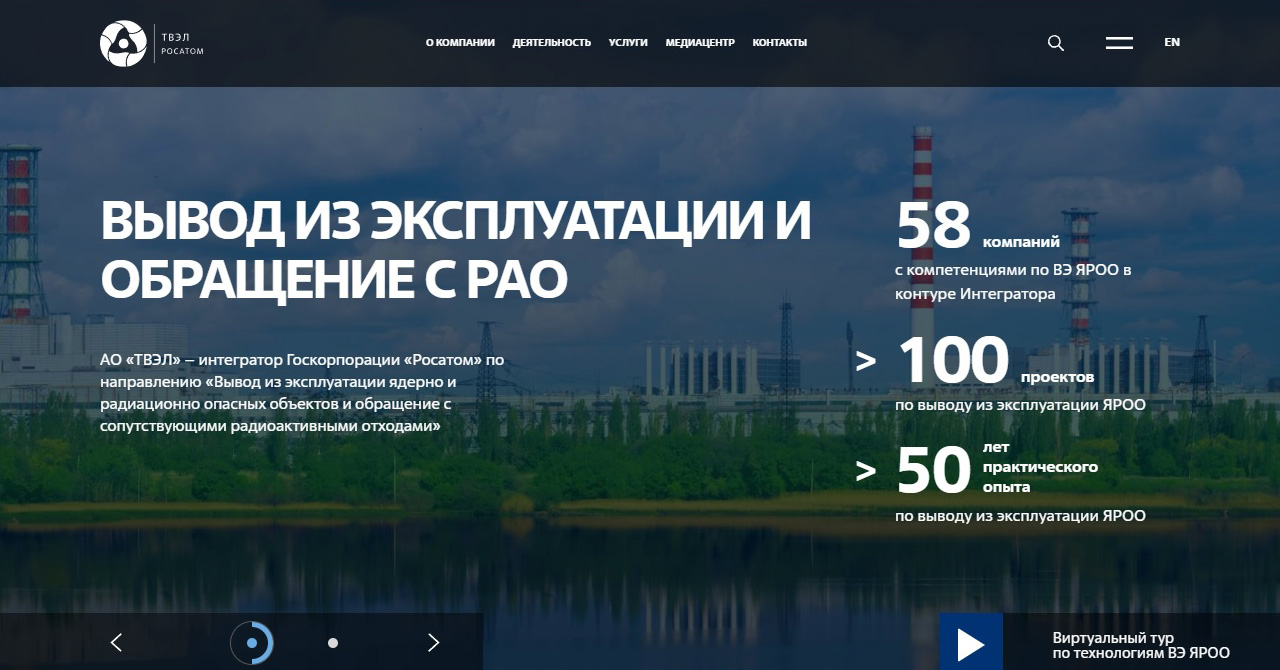
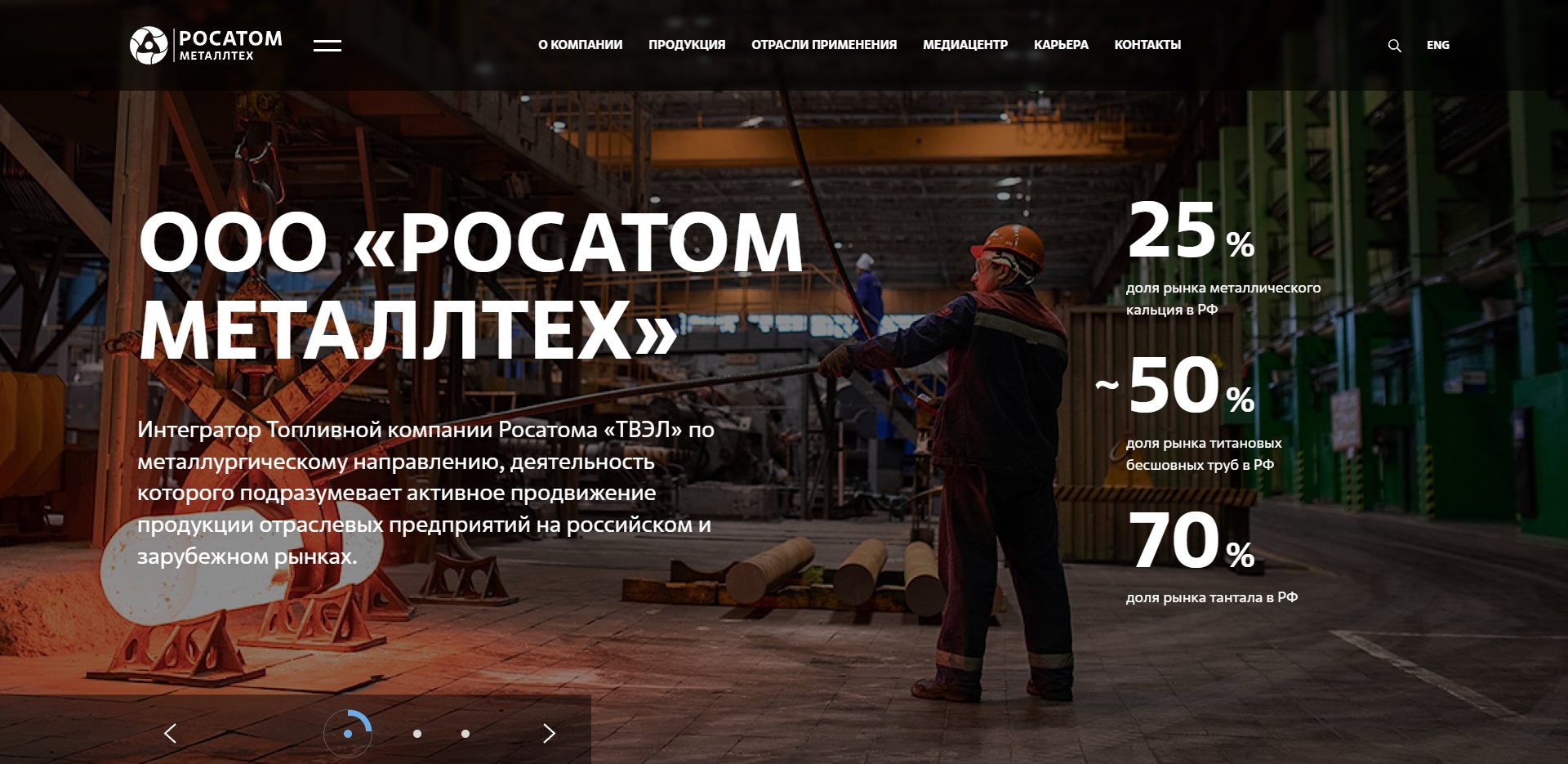
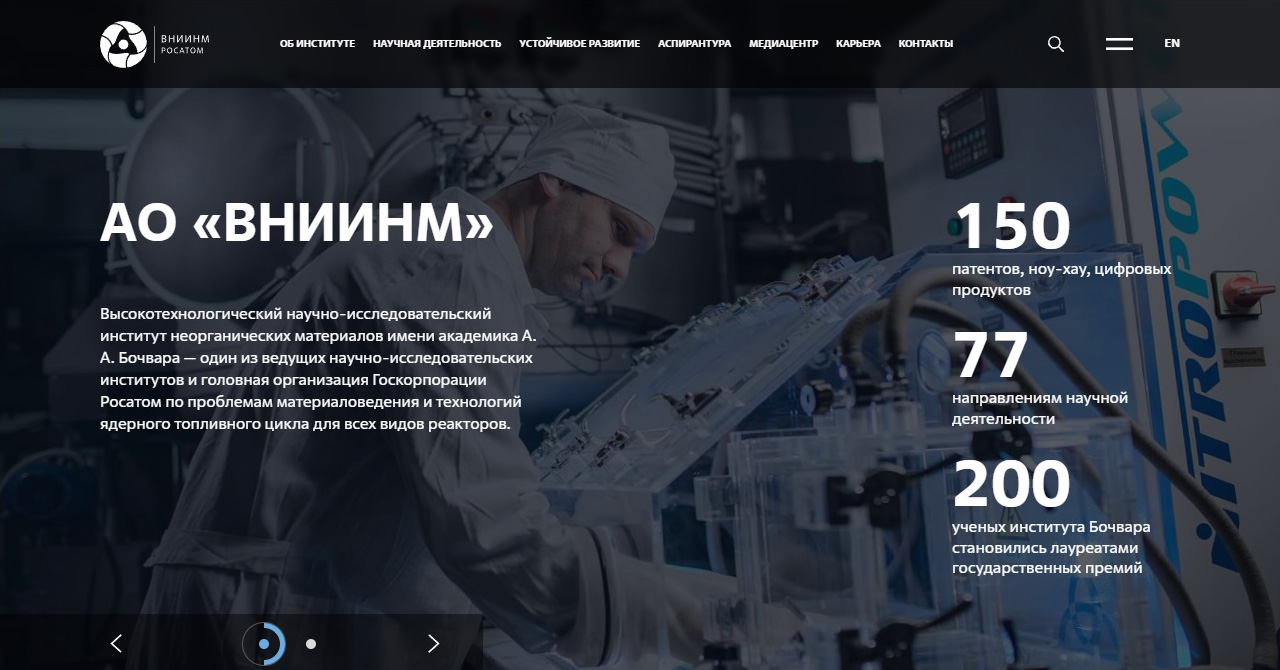
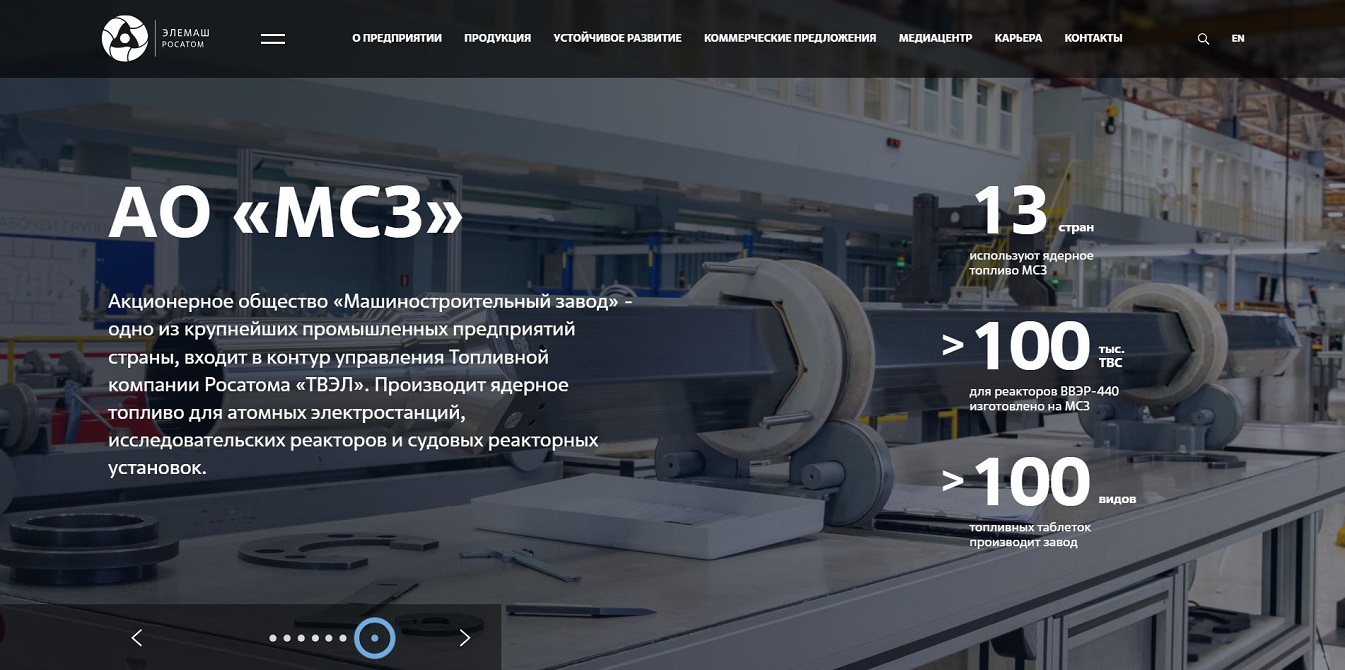
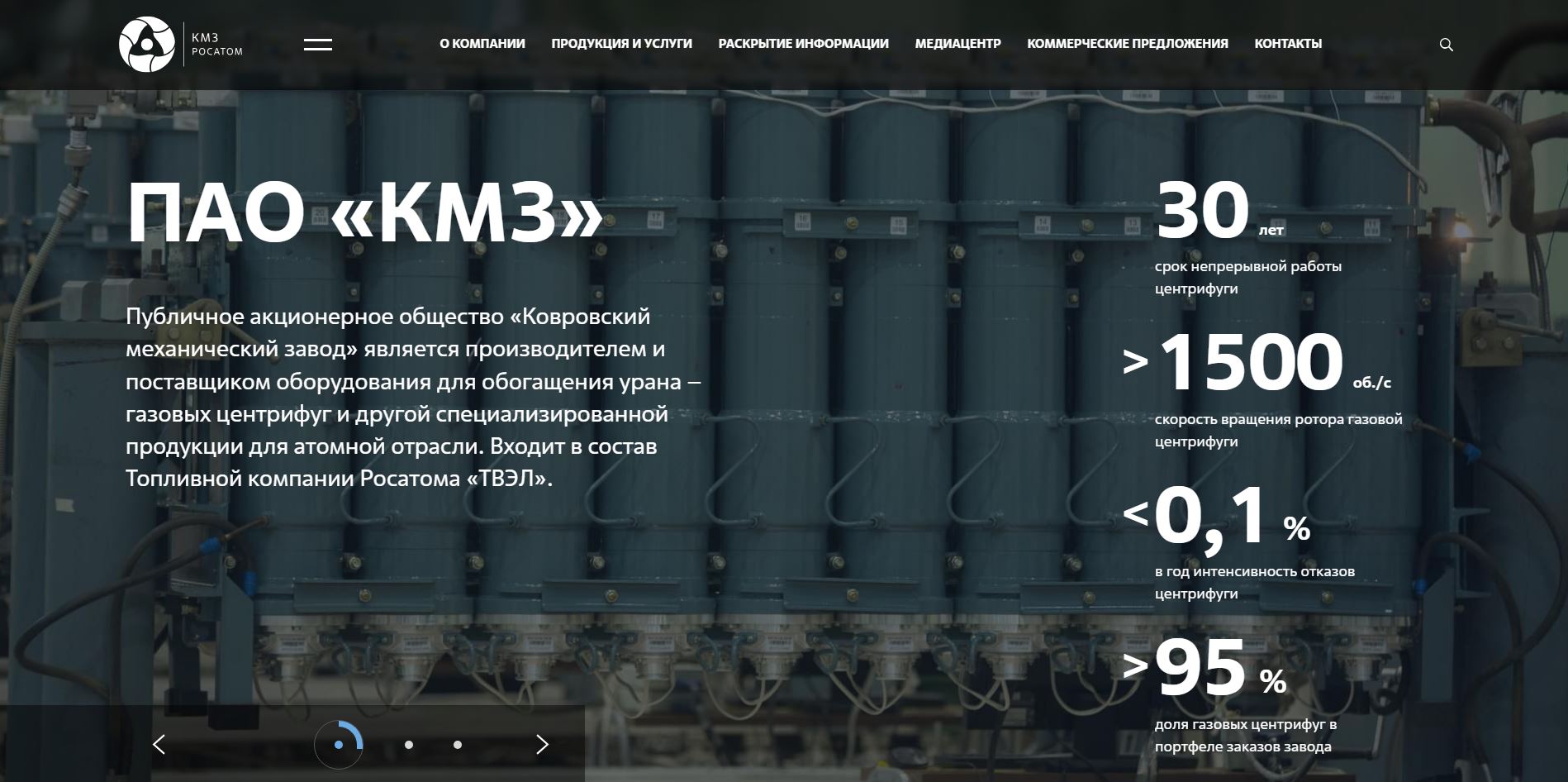
АО «ПО ЭХЗ» занимает лидирующие позиции в мире по производству изотопной продукции. Предприятие выпускает 115 стабильных изотопов 22 химических элементов и обладает значительным опытом в создании радиоизотопов высокой удельной активности. Изотопная продукция Электрохимического завода, получаемая с помощью передовой газоцентрифужной технологии, находит широкое применение в промышленности, медицине и науке.